如何判斷糖尿病類型?T1D、LADA、SIDD、MODY鑑別診斷全攻略

隨著現代糖尿病醫療的進步,傳統的二分法已經不足以應對患者的異質性。本文針對胰島素所缺乏的三大關鍵亞型:T1D(第一型糖尿病)、LADA(潛伏性自體免疫糖尿病)與 SIDD(嚴重胰島素缺乏型糖尿病)進行深度解析。
透過自體抗體(GAD/IA-2/ZnT8)判定免疫本質,並利用 C-peptide 判斷胰島功能,臨床醫師便能夠區分發病類型。不僅有助於識別立即需透過胰島素進行治療的 T1D及SIDD,也能為 LADA患者制定追蹤策略,並避免 MODY 患者接受不必要的胰島素治療。
不同類型糖尿病核心定義與關鍵差異
第一型糖尿病 (T1D)
自體免疫破壞胰島β細胞,絕對胰島素缺乏,好發兒童/青少年,需終生胰島素。
〈延伸閱讀:第一型糖尿病怎麼運動才安全?高、低血糖與酮酸中毒風險一次看!〉
LADA (Latent Autoimmune Diabetes in Adults)
成人緩慢自體免疫糖尿病,≥30歲,抗體陽性,初期不需胰島素但最終須依賴胰島素。
SIDD (Severe Insulin-Deficient Diabetes)
非自體免疫嚴重胰島素缺乏型糖尿病,常見於年輕、低BMI亞洲族群,抗體陰性,需及早使用基礎胰島素。
MODY (Maturity-Onset Diabetes of the Young)
青少年的成人發病型糖尿病,單基因糖尿病,因特定基因突變導致β細胞功能異常,呈體染色體顯性遺傳。典型發病年齡 <25歲,抗體陰性,初期不須胰島素,無酮酸中毒傾向。依亞型不同,部分患者對磺醯脲類藥物反應極佳,部分甚至不需藥物治療。
〈延伸閱讀:年輕型糖尿病YOD該怎麼逆轉?精準醫療下的五大亞型照護全攻略〉
自體抗體檢測:GAD、IA-2、ZnT8 詳解
| 縮寫 | 英文全名 | 中文名稱 | 臨床意義 |
|---|---|---|---|
|
GAD |
Glutamic Acid Decarboxylase |
麩胺酸脫羧酶 |
T1D/LADA最常見抗體 (70-80%),LADA最敏感標記 |
|
IA-2 |
Insulinoma-Associated Protein 2 |
胰島抗原2 |
特異性極高,與疾病快速進展有關 |
|
ZnT8 |
Zinc Transporter 8 |
鋅轉運蛋白8 |
60-80%新診斷T1D陽性,可補足GAD/IA-2陰性者判讀依據 |
(手機版表格可左右滑動)
檢測方式:抽血(血清),不需空腹。
方法:放射免疫沉澱法(RIA)、酶聯免疫吸附法(ELISA)、化學冷光免疫分析法(CLIA)。臨床常規組合為「糖尿病自體抗體panel」,建議診斷早期檢測。
C-peptide 臨床意義及檢測標準值
C-peptide (C肽)
胰島素原裂解產物,與胰島素等分子釋放,可穩定反映內源性胰島素分泌功能,不受外源性胰島素干擾。
C肽空腹與受刺激後參考值
| 項目 | 正常參考值 | 臨床解讀 |
|---|---|---|
|
空腹 C-peptide |
0.8 – 3.5 ng/mL |
低下 → 胰島素缺乏 |
|
刺激後 C-peptide |
通常 ≥ 2.0 ng/mL |
刺激後仍低下,確認為胰島素絕對缺乏 |
(手機版表格可左右滑動)
檢測方式:抽血檢驗(空腹或隨機),採用化學冷光免疫分析法或放射免疫分析法。不需停用外源性胰島素(因C肽不與之交叉反應)。建議在血糖穩定時檢測,避免急性高血糖或低血糖干擾結果。
鑑別閾值:空腹 C-peptide < 0.2 nmol/L(約 < 0.6 ng/mL 或 < 200 pmol/L)高度提示嚴重/絕對胰島素缺乏(T1D/SIDD);LADA 早期可能維持在較高值但逐年下降。SIDD 通常呈現嚴重缺乏(≤ 0.25 nmol/L)。MODY 通常 C-peptide 中度減低(一般 >0.2 nmol/L,但依亞型差異較大,MODY2 可接近正常,MODY3 則明顯偏低)
C-peptide 臨床決策補充
依據 Buzzetti et al. 2020 LADA 國際專家共識,隨機 C-peptide(建議在血糖穩定、無明顯低血糖或高血糖時檢測,理想範圍 80–180 mg/dL)可分為三層決策:
• < 0.3 nmol/L :視為顯著 β 細胞功能受損,按 T1D 建議採用強化胰島素方案。
• ≥ 0.3 且 ≤ 0.7 nmol/L :「灰色地帶」,採用修正後的 ADA/EASD T2D 指引,建議考慮胰島素合併其他治療以因應進行性 β 細胞衰竭,並每 6 個月追蹤 C-peptide。
• > 0.7 nmol/L : 採用修正後的 ADA/EASD T2D 指引治療,但因 LADA 可能進展,需定期監測 C-peptide。
上述三層決策係依據 Buzzetti et al. (2020) LADA 國際專家共識,主要適用於自體免疫糖尿病(T1D / LADA),對於 SIDD 或 MODY 等非自體免疫類型的直接適用性有限;其中 MODY 仍應以基因檢測確診。
針對 SIDD(嚴重胰島素缺乏型糖尿病),其 C-peptide 通常呈現嚴重缺乏(≤0.25 nmol/L),明顯低於 LADA 之灰色地帶(≥0.3–0.7 nmol/L),胰島缺乏程度與 T1D 類似。SIDD 之治療重點在於及早啟用基礎胰島素,並依餐後血糖控制情況,儘早合併餐時胰島素,以改善其較差之治療反應(Landgraf et al., 2024)。
臨床鑑別診斷重點
| 特徵 | T1D (典型) | LADA | SIDD | MODY |
|---|---|---|---|---|
|
發病年齡 |
通常 <30歲 |
通常 ≥30歲 |
華人約 40–55 歲 |
通常 <25歲 |
|
BMI |
正常或偏瘦 |
正常或偏瘦 |
正常 (較少肥胖) |
正常或偏瘦 |
|
自體抗體 |
陽性 (高) |
陽性 (GAD最常見) |
陰性 |
陰性 |
|
空腹C-peptide |
極低 (<0.2 nmol/L) |
隨病程下降 |
嚴重缺乏 (≤0.25 nmol/L) |
中度減低 |
|
酮酸中毒傾向 |
高 |
低 (後期可能) |
中至高 |
極低 |
|
疾病進展速度 |
快速 (數週~數月) |
緩慢 (數年) |
快速 (血糖嚴重升高) |
緩慢 (多數) |
|
遺傳模式 |
多基因遺傳 |
體染色體顯性 |
||
|
治療策略 |
立即胰島素 |
初期口服/GLP-1 RA |
及早基礎胰島素 |
依亞型 (部分對SU敏感) |
|
華人族群佔比 |
約 5–6% |
約 6–10% |
約 15–25% |
約 1–2% |
(手機版表格可左右滑動)
臨床鑑別診斷流程
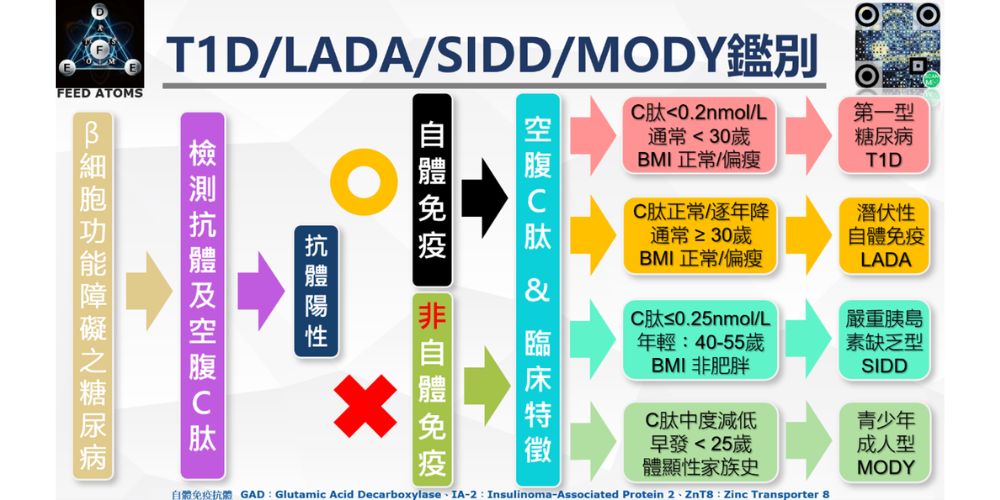
第一步 透過臨床檢測工具 (抗體 + C-peptide)進行檢測
若患者有疑似糖尿病症狀,先檢測 GAD/IA-2/ZnT8 抗體,依照檢測結果判斷為何種類型糖尿病
第二步 根據抗體結果判斷
若抗體結果呈陽性,為自體免疫:
年齡如果小於30歲,有典型症狀,可判斷為罹患T1D。
如果年齡大於等於30歲,醫生診斷後6個月不需胰島素,則可判斷為罹患LADA。
若抗體結果呈陰性,為非自體免疫:
要透過空腹C-peptide & 臨床特徵進行判斷,若患者年輕(40-55歲)、BMI正常、C-peptide極低(≤0.25 nmol/L),則可判斷為罹患SIDD。
早發(<25歲)、C-peptide 中度減低、有體染色體顯性家族史(連續三代) → 高度懷疑 MODY,建議基因檢測確診。
〈延伸閱讀:糖尿病檢測怎麼做?揪出不同糖尿病類型,及早預防併發症!〉
臨床鑑別要點總結
第一步 檢測GAD抗體
陽性指向自體免疫 (T1D/LADA);陰性往非免疫胰島素缺乏評估。
第二步 評估C-peptide與臨床軌跡
- 年輕+抗體陽性+嚴重高血糖 → T1D
- 成人+抗體陽性+6個月不需胰島素 → LADA
- 抗體陰性+C-peptide極低+非肥胖 → SIDD。
- 抗體陰性 + 早發(<25歲) + C-peptide 中度減低 + 體顯性家族史 → MODY
第三步 治療反應
SIDD對基礎胰島素反應較差(Landgraf et al., 2024 中僅 19–22% 達標),常需及早強化治療(包含餐時胰島素),對 Sulfonylureas(磺醯脲類)/GLP-1 RA療效有限;LADA早期可嘗試GLP-1 RA但需追蹤C-peptide。MODY 的治療依基因亞型而定:MODY2 通常不需藥物;MODY3 及 MODY1 對磺醯脲類藥物反應極佳,應避免不必要的胰島素治療。
所有成人新診斷糖尿病且體型消瘦、HbA1c極高、無典型代謝症候群者,建議常規檢測抗體及C-peptide。若有明顯家族遺傳史且發病年齡極早,應考慮 MODY 並轉介基因檢測。
關鍵輔助檢測參數
| 檢測項目 | T1D / LADA | SIDD | MODY | 臨床建議 |
|---|---|---|---|---|
|
GAD抗體 |
陽性 |
陰性 |
陰性 |
一線篩檢 |
|
空腹C-peptide |
<0.2 nmol/L |
≤0.25 nmol/L |
中度減低 |
嚴重缺乏 → 胰島素優先 |
|
HLA基因型 |
高風險 (DR3/DR4) |
無特定 |
無特定 |
研究用途 |
|
酮體 |
易有酮酸中毒 (DKA) |
高血糖時可能酮酸 |
不易酮酸中毒 |
預防 DKA |
|
基因檢測 |
不需要 |
不需要 |
診斷黃金標準 |
MODY 確診 |
(手機版表格可左右滑動)
治療策略摘要
T1D
基礎-餐時胰島素 「每日多次胰島素注射(Multiple Daily Injections, MDI)」或胰島素幫浦,搭配CGM。
〈延伸閱讀:糖化血色素(HbA1c)是什麼?帶你掌握血糖控制的關鍵!〉
LADA
早期Metformin / DPP-4i / GLP-1 RA,定期監測C-peptide,血糖惡化即啟用胰島素。
SIDD
SIDD 亞群對基礎胰島素反應較差。Landgraf et al. (2024) 的 EDITION 3 post-hoc 分析顯示,即使使用較高劑量基礎胰島素(0.7–1.0 U/kg/day)或已合併餐時胰島素,僅有 19–22% 的 SIDD 患者能在 26 週達到 HbA1c < 7.0% 目標(明顯低於其他亞型),且最終 HbA1c 仍常維持在 7.7–8.0%,主要因餐後血糖控制不佳所致。
因此強烈建議及早啟用基礎胰島素,並盡早優化餐時胰島素劑量或其他強化治療(Landgraf et al., 2024)。延遲胰島素強化與心血管事件風險增加有關(Gavin et al., 2023;Khunti et al., 2024)。
若患者合併心血管或腎臟疾病,可考慮依共病狀況加用 SGLT2 抑制劑(優先)或 GLP-1 受體促效劑。此建議主要基於一般 T2D 人群的證據。
2025 年真實世界研究(Tsur et al., 2025)顯示 SGLT2i 在胰島素缺乏型糖尿病患者仍能提供顯著腎臟保護,其中primary outcome:HR 0.79,顯示用藥組的腎功能惡化(如腎衰竭、肌酸酐翻倍、洗腎或死於腎病)的風險,比不用藥組降低了 21%; Creatinine Doubling(肌酸酐加倍):HR 0.76,因為肌酸酐是反映腎功能的指標,翻倍代表腎功能嚴重衰退,而SGLT2i 讓肌酸酐翻倍的風險降低了 24%。且白蛋白尿改善達 51%),DKA 發生率雖較對照組略高(2.81% vs 2.19%),但整體發生率低且可透過適當監測管理(Tsur et al., 2025)。
MODY
治療策略依基因亞型而定:
MODY2 (GCK 突變):通常僅輕微空腹高血糖,不增加長期併發症風險,一般不需藥物治療,僅需飲食控制及定期追蹤。
MODY3 (HNF1A 突變):對磺醯脲類藥物反應極佳,可作為首選治療,應避免不必要的胰島素注射。
MODY1 (HNF4A 突變):同 MODY3,對磺醯脲類敏感。
其他罕見亞型:依個別基因功能選擇治療方式。
所有 MODY 確診均需仰賴基因檢測,正確分型可避免錯誤治療(如將 MODY3 誤診為 T1D 而長期使用胰島素)。
〈延伸閱讀:胰島素阻抗指標(HOMA-IR)要當心!胰島素阻抗之定義、計算與臨床應用一次掌握!胰島素阻抗指標HOMA-IR解析〉
結論
T1D、LADA、SIDD皆為胰島素缺乏,但病因與治療策略不同:
T1D:自體免疫、抗體陽性、C-peptide極低,需立即MDI(基礎‑餐時胰島素)。
LADA:成人緩慢自體免疫,抗體陽性,初期可不用胰島素,但須追蹤C-peptide,惡化時需胰島素治療。
SIDD:抗體陰性、年輕低BMI、C-peptide嚴重缺乏,對基礎胰島素反應差(僅19‑22%達標),需及早啟用較高劑量基礎胰島素並合併餐時胰島素。
MODY:單基因遺傳、抗體陰性、C-peptide 中度減低,發病年齡 <25 歲且有體顯性家族史,治療依亞型而異(MODY2 不須藥物,MODY3 對磺醯脲類敏感),應以基因檢測確診。
鑑別四步驟:檢測GAD抗體 → 評估空腹C-peptide → 結合年齡、BMI、酮酸傾向。延遲胰島素強化會大幅增加心血管風險(心衰竭+64%,心肌梗塞+67%)。精準分型才能避免治療惰性,及時使用最適方案,避免不必要的胰島素注射(尤其 MODY)。
參考資料
- Ahlqvist, E., et al. (2018). Novel subgroups of adult-onset diabetes and their association with outcomes: A data-driven cluster analysis of six variables. The Lancet Diabetes & Endocrinology, 6(5), 361–369.
- Li, X., et al. (2020). Identification of type 2 diabetes subgroups in the Chinese population. The Journal of Clinical Endocrinology & Metabolism, 105(10), dgaa524.
- Jones, A. G., et al. (2016). Markers of β-cell failure predict poor glycemic response to GLP-1 receptor agonist therapy in type 2 diabetes. Diabetes Care, 39(2), 250–257.
- Leslie, R. D., et al. (2018). Adult-onset autoimmune diabetes: Current knowledge and future perspectives. Diabetologia, 61(12), 2473–2482.
- Buzzetti, R., et al. (2020). Management of latent autoimmune diabetes in adults: A consensus statement from an international expert panel. Diabetes, 69(10), 2037–2047.
- American Diabetes Association. (2026). 2. Diagnosis and Classification of Diabetes: Standards of Care in Diabetes—2026. Diabetes Care, 49(Suppl. 1), S27–S49.
- Luo, S., et al. (2024). Early insulin treatment and cardiovascular outcomes in newly diagnosed type 2 diabetes: A real-world evidence study. Signal Transduction and Targeted Therapy, 9(1), 154.
- Rosenstock, J., et al. (2018). More similarities than differences testing insulin glargine 300 U/mL versus insulin degludec 100 U/mL in insulin-naive type 2 diabetes: The randomized head-to-head BRIGHT trial. Diabetes Care, 41(10), 2147–2154.
- Cheng, A. Y. Y., et al. (2024). Efficacy and safety of insulin glargine 300 U/mL in insulin-naive people with type 2 diabetes with/without prior use of GLP-1 receptor agonist therapy. Diabetes Research and Clinical Practice, 217, 111871.
- Tuomi, T., et al. (2014). The many faces of diabetes: A disease with increasing heterogeneity. The Lancet, 383(9922), 1084–1094.
- Jones, A. G., & Hattersley, A. T. (2013). The clinical utility of C-peptide measurement in the care of patients with diabetes. Diabetic Medicine, 30(7), 803–817.
- Landgraf, W., et al. (2024). Treatment responses to basal insulin glargine 300 U/mL and glargine 100 U/mL in newly defined subphenotypes of type 2 diabetes: A post hoc analysis of the EDITION 3 trial. Diabetes, Obesity and Metabolism, 26(2), 503-511.
- Khunti, K., et al. (2024). Effect of delay in treatment intensification in people with type 2 diabetes and suboptimal glycaemia after basal insulin initiation. Diabetes, Obesity and Metabolism, 26(3), 1062-1071.
- Gavin, J. R., et al. (2023). Therapeutic inertia and delays in insulin intensification in type 2 diabetes: A literature review. Diabetes Spectrum, 36(4), 379-384.
- Ou, S. M., et al. (2025). Comparative outcomes of adding SGLT2 inhibitors versus incretin-based therapies to insulin in type 2 diabetes. Diabetes Research and Clinical Practice, 212, 111938.
- Tsur, A., et al. (2025). Kidney outcomes with SGLT2 inhibitors in patients with diabetes and an insulin-deficient phenotype: A real world analysis. Diabetes, Obesity and Metabolism, 27(6), 3176–3184.
- Fajans, S. S., & Bell, G. I. (2011). MODY: history, genetics, pathophysiology, and clinical decision making. Diabetes Care, 34(8), 1878-1884.
- Shields, B. M., et al. (2017). Population-based assessment of a biomarker-based screening pathway to aid diagnosis of monogenic diabetes in young-onset patients. Diabetes Care, 40(8), 1017-1025.


