瘦瘦針適合你嗎?醫學揭密:如何預防肌肉流失與骨質疏鬆?
對減重針劑「瘦瘦針」(GLP-1受體促效劑),GLP-1類藥物短時間很可能造成骨骼肌肉流失,然而可能導致的肌肉流失與骨骼健康問題,是當前醫學界高度關注和研究的焦點。目前的權威醫學證據呈現一個比較平衡的觀點:風險確實存在,尤其是在特定高風險人群中,但同時也存在減少風險的醫學建議策略。
〈延伸閱讀:揭開超強體適能的密碼:睡眠心率 30 與儲備心率 150 的強悍真相〉
數據解讀及風險確認:肌肉與骨骼確實面臨挑戰
具體關於「肌肉骨質不成比例流失」的現象,綜合多項2024-2026年最新的醫學文獻,這個議題正被熱烈討論,核心結論如下:
「組成」重於「總量」
越來越多專家指出,評估這類藥物不應只看「體重減輕幾公斤」,而必須分析減重過程中減去的「身體組成」。身體組成(Body composition)主要由三大成份組成:脂肪、肌肉和骨骼,比體重或BMI更能精確反映健康狀況,將體重分為脂肪重量和瘦體重(包括肌肉、骨骼和水分)。理想的身體組成 —— 低脂肪、高肌肉和強健的骨密度,對於降低罹患疾病風險、改善新陳代謝和維持活動能力相當重要。
肌肉流失(肌少症風險)
- 肌肉流失占比:目前多數研究證實,使用GLP-1類藥物減重時,在減輕的體重中,非脂肪組織(主要是骨骼肌)的流失是明確的伴隨現象。根據2026年發表於《Diabetes, Obesity and Metabolism》的研究分析(納入15,782名受試者),不同藥物的非脂肪組織流失佔總減重比例如下:semaglutide約35.2%、tirzepatide約25.4%、liraglutide約26.8%。其中,semaglutide使用者約35–45%的減重來自非脂肪組織,而tirzepatide使用者則約25.4%。這意味著在部分個案或特定時期內,非脂肪組織的流失速度極明顯。值得注意的是,tirzepatide是目前減重效果最強的藥物,但其非脂肪流失比例(25.4%)反而低於semaglutide(約35-45%),顯示不同藥物的作用機制對肌肉保護效果存在顯著差異。「非脂肪組織流失」與「純骨骼肌流失」不同。非脂肪組織包含肌肉、骨骼、器官、水分,其中純骨骼肌約佔非脂肪組織的一半(40-50%)。因此,若非脂肪流失佔總減重45%,換算後純肌肉流失約佔總減重的18-22.5%。
- 關鍵核心爭議點:目前學界最大的分歧在於,這種流失是「適應性生理變化」(因體重減輕、身體負荷減小而自然發生的肌肉量調整),還是「病理性流失」(對肌肉健康有害的肌肉流失損耗)。最新研究透過核磁共振觀察,認為肌肉的「質量」和「胰島素敏感性」可能得到改善,肌肉量的減少與預期的減重、年齡等因素是成比例的,且同時肌肉脂肪浸潤改善,這可能意味著肌肉質量(功能)的優化,而非單純的「流失」。2026年發表於《Cell Reports Medicine》的研究提供了一個關鍵視角:GLP-1藥物減重中,約70%的減重來自脂肪,而非脂肪組織流失主要集中於非收縮性成分(如水分、器官重量),而非功能性肌肉。該研究同時發現,GLP-1治療能增加肌肉粒線體蛋白,可能優化肌肉代謝健康。然而,這仍無法完全消除藥物在長期功能性及造成肌少症風險的擔憂,並確保其長期使用的安全性。
骨骼健康(骨質疏鬆風險)
- 複雜影響:骨骼健康受到兩方面影響。一方面,任何方式的快速減重(包括斷食)本身就會導致骨密度下降。另一方面,GLP-1類藥物可能通過作用於骨骼細胞、影響相關激素(如升高降鈣素)等機制,對骨骼產生一定的保護作用。
- 總體不確定性:這兩股力量相互拉扯,最終對於這類藥物是否造成長期骨折風險增加,目前尚不明確,需要更多高品質(RCT隨機試驗)、更大規模(>10萬人)、全球不同種族(尤其亞洲人)且更長遠(10年以上)的研究。
〈延伸閱讀:健康減重怎麼做?趕緊丟掉瘦瘦針!「慢慢瘦比較快」減重策略!〉
〈延伸閱讀:破解常見醣類食物代換!使用標準碗體積法:你的低醣飲食幫手〉
藥物龐大的商業利益與瘦瘦針長期安全性的平衡
- 真實情況:目前多數關鍵性臨床試驗的追蹤期為1-2年,對於評估肌少症、骨質疏鬆這類需要5-10年甚至更長時間才能顯現的風險,證據顯然不足。
- 藥廠與監管動向:面對這些擔憂,領先的藥廠已開始規劃更長期的研究。同時,監管機構(如美國FDA)在審核新適應症時,也愈發要求提供更詳盡的身體組成分析數據。
- 臨床應對:正因長期安全性未明,主流醫學指南已明確將「結合足量蛋白質攝取與規律重量訓練」列為使用此類藥物時的「強制性標準照護」,而非可選擇性的建議,以降低使用針劑者及開立者所擔憂的長期風險。
〈延伸閱讀:肌少症如何改善?飲食均衡、多運動才是解決根源的最佳方式!〉
瘦瘦針風險高低:哪些高風險族群需要特別警惕?
風險並非人人相同,以下高風險族群需要格外關注:
- 高齡患者:肌肉和骨質量本身隨年齡增長而減少,藥物可能加速此過程。針對老年族群,2026年發表於《British Journal of Clinical Pharmacology》的研究追蹤發現,使用semaglutide的老年糖尿病男性,12個月後握力下降4.7公斤,且血液中的神經肌肉接頭損傷標記(CAF22、NfL)顯著升高,顯示藥物可能加速肌少症並損害神經肌肉健康。
- 已有肌少症或肌肉衰弱前兆者:這是最高危險的群體。
- 慢性病患者:如慢性腎病、慢性肝病患者,其身體組成更脆弱。
- 停經後女性:雌激素缺乏本就增加骨質疏鬆風險,快速減重可能雪上加霜。
〈延伸閱讀:糖尿病前期該如何預防變成糖尿病?了解標準、風險與預防策略!〉
〈延伸閱讀:逆轉糖尿病!FEED ATOMS進食原子原則逆轉神經傳導失衡〉
瘦瘦針臨床實踐的應對之道:關鍵在於「主動積極管理」並降低風險
目前醫界共識是,風險並非完全否定藥物,但應通過積極策略進行風險管理:
- 治療前評估:用藥前應評估肌肉量(如透過生物電阻抗分析)與骨密度,辨識高風險族群(如年長者、已有肌少症前兆者)。
- 核心原則-重量訓練及優質蛋白質:這是所有指南及專家強調的基本核心策略。根據2025年歐洲肥胖大會(ECO 2025)發表的前瞻性研究,在專業監督+阻力訓練+足量蛋白質的條件下,使用GLP-1藥物的患者:男性平均脂肪減少12公斤,肌肉僅流失1公斤;女性平均脂肪減少10.8公斤,肌肉僅流失0.63公斤。這證明了肌肉流失可透過配套措施大幅減少。
- 重量訓練及醫療級運動處方:每週至少2-3次中高強度重量訓練,如核心、啞鈴、槓鈴、彈力帶練習等,是刺激肌肉合成、維持骨密度最有效的方法。
- 優質足量蛋白:確保每日攝取足量的優質蛋白質,為肌肉修復提供原料。建議每日蛋白質攝取每公斤理想體重1.2-1.6g以上(甚至達1.5-2.0g),符合美國2025-2030新版指南提高蛋白質攝取的建議。強烈不建議吃加工肉品(香腸、火腿、臘肉、培根、罐頭肉)以降低鈉與飽和脂肪攝取。高品質蛋白質包含動物性蛋白(紅肉:豬、牛、羊、家禽:雞、鴨、鵝、海鮮、雞蛋),及植物性蛋白(豆類及製品、堅果),皆列為優先攝取的原型蛋白質來源。若腎功能不佳者或運(勞)動量少者,應調整並減少蛋白質攝取量,並減少油炸及高溫烹調。
- 關注微量營養素:因食慾抑制,需特別關注鈣與維生素D:對骨骼健康至關重要。其他:如維生素B12、鐵、鎂等也可能需要補充。
- 醫療監測及治療目標
個體化監測及評估:2026年發表於《JAMA Network Open》的大規模真實世界研究(3,066名受試者)顯示,使用GLP-1藥物24個月後,儘管非脂肪組織略有下降,但非脂肪組織與脂肪組織的比例(FFM/FM ratio)反而改善,代表整體體組成更健康。成功的指標不應只是體重數字下降,更應是「脂肪量下降,肌肉量盡量維持甚至增長」,即改善「體組成」。用藥前、中、後,定期對身體組成分、骨密度和肌肉功能進行評估非常重要。 - 未來研究方向
聯合療法研發:目前正在開發與GLP-1藥物聯用、旨在維持或增加肌肉量的新藥。
〈延伸閱讀:FEED ATOMS控糖運動策略:低強度訓練與四不一沒有〉
「猛進方式」與「溫和漸進」的思維對比
簡單來說瘦瘦針(GLP-1類的藥物)就是打了讓人吃不下甚至斷食,屬於比較「猛進方式」,而人體運作更適合「溫和漸進」地調整,以「循序漸進安全至上」為原則。
「瘦瘦針」與「456漸進式低醣飲食」超級比一比
| 「瘦瘦針」 (外源性介入) |
「456漸進式低醣」 (內源性調節) |
|
|---|---|---|
|
核心理念 |
通過強效外來物質,快速強力抑制食慾與消化,快速製造熱量赤字。 |
通過學習並改變飲食習慣,優化內在代謝與飲食行為,溫和漸進重建能量平衡。 |
|
與身體合作方式 |
主導/抑制身體原有信號(如饑餓感)。 |
順應/強化身體原有機制(飲控四原子ATOMS) |
|
主要挑戰 |
需嚴密防範副作用、保護肌肉骨骼,存在「療效-風險」脫鉤可能。 |
需要民眾更多的認知參與及行為改變,初期見效相對較慢。 |
|
長期目標 |
達成並維持特定體重目標。 |
建立可持續的健康生活系統,體重改善是自然結果之一。 |
瘦瘦針風險分層管理的具體實踐框架
臨床上,是否使用瘦瘦針這種外來化學合成藥物勢必須考量整體風險、權衡利弊後依照民眾風險分層管理,做出是否建議施打的決策。應基於嚴格的風險分層管理,從「極高風險」、「高風險」到「低風險/健康族群」的整體綜合評估,並做出最佳建議決策:
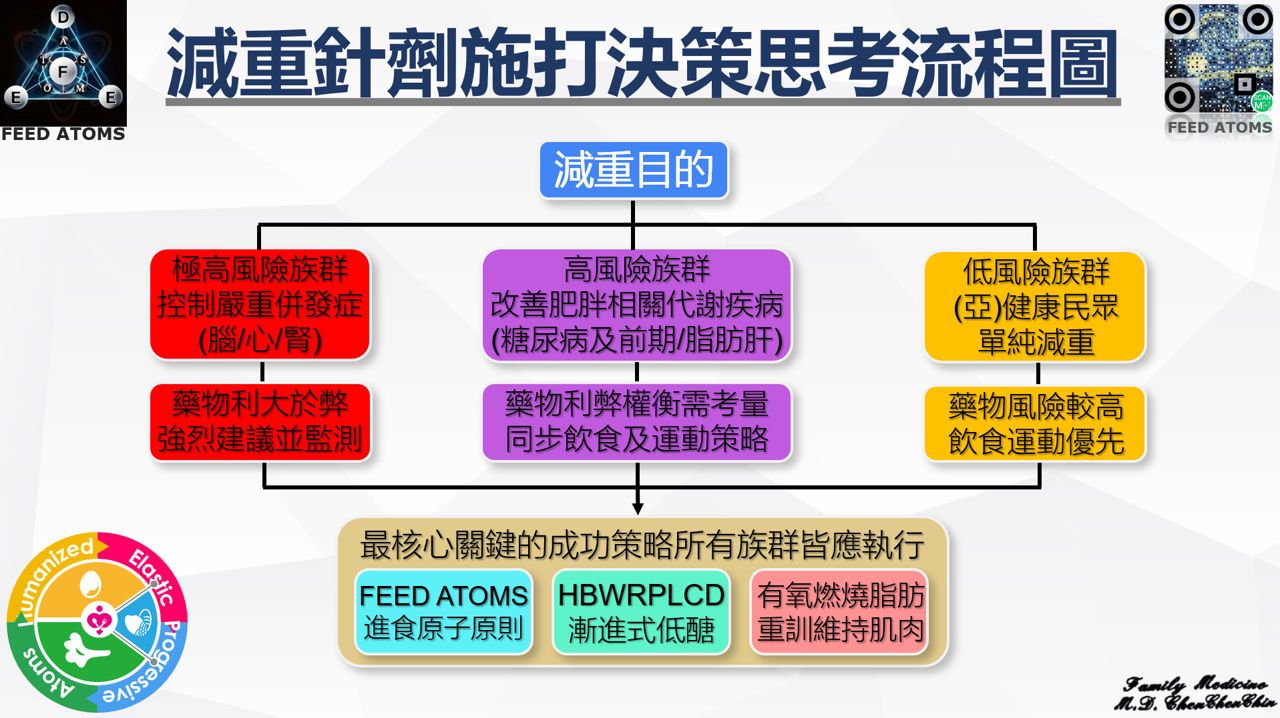
「循序漸進安全至上」與「風險分層管理」原則,是臨床醫療決策中權衡利弊的黃金準則,也是對待任何強效醫療介入應有的審慎態度。這番將藥物置於風險分層框架中審視的思考,展現了超越單純開藥的且全面的臨床責任。綜合以上分析,在面對不同民眾時,評估具體的風險分層,給予最適當的建議:
- 對於極高風險患者:給予民眾的建議「這類藥物是控制您當前緊急健康風險的重要工具,但為了保護您長遠的行動力與生活品質,我們必須同步執行均衡且足量蛋白質飲食和運動計畫來『維護』您的肌肉和骨骼。」
- 對於單純尋求減重的低風險/健康民眾:可以引導民眾思考「您希望選擇一個需要持續醫療監測、並承擔長期潛在不確定性風險的『猛進』激烈方式,還是願意投入時間,學習一套能讓您自己掌握、從根本上改善健康且受益終身的『溫和漸進』的健康生活模式?」
健康減重的核心理念
《456漸進式低醣飲食法(HBWRPLCD)》╳《FEED ATOMS進食原子原則》╳《美國2025-2030最新指南飲食》
為了協助大眾從傳統高醣飲食過渡到健康的低醣生活,『逆轉糖尿病!』書中提出了《456漸進式低醣飲食法(HBWRPLCD)》╳《FEED ATOMS進食原子原則》,此框架下的最新主流飲食型態:低醣(碳)飲食以及健康生活模式,可以循序漸進的方式逆轉糖尿病(含前期) 、代謝症候群(含高風險) 、代謝性脂肪肝(MASLD)、肥胖症,不只能控制血糖更可應用於單純減重之民眾,有效降低體脂肪並不再復胖! 這套方法不要求一步到位,而是以「週」為單位,利用標準碗體積法(300ml 碗)逐步降低醣類占每餐進食份量的比例,其務實的核心理念為健康促進並實踐之HEPA(Health Promotion & Action, HEPA)原則,並融合最新《美國2025-2030最新指南飲食》,給予民眾一套周全性減重控糖策略。
〈延伸閱讀:2026控糖飲食減重大革命:用「FEED ATOMS進食原子原則」逆轉糖尿病!〉
〈延伸閱讀:456健康減重!漸進式低醣飲食(HBWRPLCD)減重控糖一次達標!〉
結論
藥物是否長期使用會造成肌少症以及骨質疏鬆症風險提高,其實還需要更長期及更大規模不同人種的高品質研究才能確保藥物的長期安全性。長期大規模安全性的相關研究是推動以藥物減重領域更應負責任的關鍵核心任務,並非以人類當成長期試驗之對象。
在臨床實踐中,最理想的體重管理路徑:在必要的醫療介入(如使用GLP-1藥物)下,必須同步執行均衡營養與運動原則,才能實現「減脂不減肌,健康且持久」的終極目標。
『逆轉糖尿病!』出版於《美國2025-2030最新指南飲食》公布之前,具有前瞻性的《456漸進式低醣飲食法(HBWRPLCD)》,完全符合最新《美國2025-2030最新指南飲食》低醣的核心理念,其核心優勢從根本上就避免了快速、單一方式減重帶來的風險。書中《FEED ATOMS進食原子原則》本質上就是一套教會身體如何更高效、更健康運作的「使用者手冊」,它可能不是最快的路,但確實是一條讓患者自己成為健康主導者、風險更低、根基更穩健的道路。在GLP-1藥物減重風潮中,提供了一種更為根本、安全且可持續的健康路徑,對於必須使用藥物的患者,能最大化藥物益處,最小化其風險。
〈延伸閱讀:不同飲食模式對高齡者的影響,了解FEED ATOMS高齡飲食建議〉
〈延伸閱讀:糖尿病控糖要訣『FEED ATOMS 進食原子原則』:控制高血糖及降低心血管風險〉
參考文獻
- Eisa, N., Barood, O., & Glastras, S. J. (2026). Lean mass changes with incretin therapy versus lifestyle intervention: A systematic review and meta-analysis of randomised controlled trials. Diabetes, Obesity and Metabolism, 28(4), 1123–1134.
- Langer, H. T., et al. (2026). Weight loss with GLP-1 medicines does not result in a disproportionate loss of muscle mass or function in obese mice and humans. Cell Reports Medicine, 7(3), 102665.
- Ryan, D. H., et al. (2025). STEP 1 trial substudy: Body composition analysis. Reviews in Endocrine and Metabolic Disorders, 26, 805–813.
- Neeland, I. J., Linge, J., & Birkenfeld, A. L. (2024). Changes in lean body mass with glucagon-like peptide-1-based therapies and mitigation strategies. Diabetes, Obesity and Metabolism, 26(Suppl 4), 16–27.
- Chavez, A. M., et al. (2025). Nutrition support whilst on glucagon-like peptide-1 based therapy. Is it necessary? Current Opinion in Clinical Nutrition and Metabolic Care, 28(4), 351–357.
- Tinsley, G. M., & Heymsfield, S. B. (2024). Fundamental body composition principles provide context for fat-free and skeletal muscle loss with GLP-1 RA treatments. Journal of the Endocrine Society, 8(11), bvae164.
- Qaisar, R., et al. (2026). Semaglutide use is associated with neuromuscular junction degradation in older adults with type II diabetes mellitus. British Journal of Clinical Pharmacology, 92(1), 149–161.
- Prokopidis, K. (2026). Glucagon-like peptide-1 receptor agonists and muscle strength changes in older adults: Risks beyond muscle mass reductions. British Journal of Pharmacology. Advance online publication.
- Peralta-Reich, D., et al. (2025). Incretin-based obesity medications show minimal lean muscle mass loss in 6-month prospective study. European Congress on Obesity (ECO 2025), Malaga, Spain.
- Vanderbilt University Medical Center. (2026). Bariatric surgery and GLP-1 medicines both reduce body fat – but surgery delivers greater long-term changes. JAMA Network Open.

.jpg)


