糖尿病控糖要訣『FEED ATOMS 進食原子原則』:控制高血糖及降低心血管風險

第二型糖尿病控制血糖最關鍵的四要素『FEED』:食物(Food)、運動(Exercise)、減重/減脂(Eliminate weight/fat)以及藥物(Drugs)。其中飲食控制的四個原子『ATOMS』餐食的總量、種類、順序及進食速度(amount, type, order of meals and eating speed),自創共同組成英文縮寫為:『FEED_ATOMS(進食_原子)原則』。
執行『FEED_ATOMS(進食_原子)原則』,飲食控制落實在每日、每一餐、每一口,搭配規律運動及適當減重減脂,並遵照醫囑使用降血糖藥物,血糖控制將可達成,以減少血管發炎及內皮功能障礙,預防及延緩動脈粥狀硬化,降低心血管疾病風險。
歡迎點擊查看發表於內科學誌全篇論文:糖尿病控糖要訣『FEED_ATOMS(進食-原子)原則』
第二型糖尿病的影響、風險及FEED_ATOMS控糖原則
第二型糖尿病 (Type 2 Diabetes, T2D) 的病理生理進程包括代謝症候群和糖尿病前期,第二型糖尿病與顯著的心血管疾病(Cardiovascular disease, CVD)風險相關聯,而合併代謝症候群會使 CVD 風險增加近 5 倍,以下將會介紹相關影響與風險。
〈延伸閱讀:糖尿病前期該如何預防變成糖尿病?了解標準、風險與預防策略!〉
〈延伸閱讀:糖尿病檢測怎麼做?揪出不同糖尿病類型,及早預防併發症!〉
代謝症候群的影響
代謝症候群 (metabolic syndrome)包括腰圍大、高血糖、高血壓、高三酸甘油脂和高密度脂蛋白膽固醇過低,通常伴隨著全身慢性發炎,發炎反應會導致促炎細胞激素(Proinflammatory cytokines)的釋放,促進第二型糖尿病的進展,細胞激素會進一步損害血管內皮,促進動脈粥狀硬化(atherosclerosis)進展,增加CVD風險。
〈延伸閱讀:代謝症候群(Metabolic syndrome)的定義為何?本篇帶你認識這個「潛在的慢性健康殺手」!!〉
高血糖與血管損傷
高血糖會透過晚期糖基化終產物 (advanced glycosylated end products) 和氧化壓力 (oxidative stress) 等因素促進心血管疾病的發展。胰島素阻抗和高血糖都會促進冠狀動脈疾病、腦血管疾病和心臟衰竭的發生。第二型糖尿病中的動脈粥狀硬化性血脂異常 (atherogenic dyslipidemia) 與慢性低度血管發炎 (chronic low-level vascular inflammation) 和促血栓狀態 (prothrombotic state) 相關。
〈延伸閱讀:胰島素阻抗指標(HOMA-IR)要當心!胰島素阻抗之定義、計算與臨床應用一次掌握!胰島素阻抗指標HOMA-IR解析〉
生活方式與藥物治療的重要性
生活方式干預的重要性:
飲食、運動和減重在改善血糖及 CVD 風險方面發揮著至關重要的作用。
藥物治療:
Sodium-Glucose Transport Protein 2 Inhibitors (SGLT-2Is)降低血糖、降低體重、降低血壓,顯著改善第二型糖尿病患者的心血管和腎臟預後。
Glucagon-Like Peptide-1 Receptor agonists(GLP-1Ras)降低血糖、降低體重、降低血壓,在具有心血管風險的第二型糖尿病患者的管理中佔有重要的地位。
糖尿病自我管理教育(DSMES)
2024年美國糖尿病協會(American Diabetes Association)強烈鼓勵所有糖尿病患者參與糖尿病自我管理教育和支持(Diabetes Self-Management Education and Support, DSMES) ,例如:健康飲食、身體活動、服用藥物等,以促進知情同意並決策、自我保健及照護、解決問題能力以及與醫療團隊的積極合作。醫學營養治療(medical nutrition therapy)可以節省成本並改善心臟疾病風險。對於所有超重或肥胖的人,建議行為改變以實現並維持至少5%的體重減輕。對於糖尿病前期或糖尿病患者的糖尿病預防與管理,推薦個人化的飲食計劃,注重營養品質、總熱量和代謝目標。針對代謝症候群進行飲食和生活方式的調整,有助於減少血管發炎,降低心血管疾病的風險。
FEED_ATOMS進食原子原則
醫學生養成教育中常常學習許多英文口訣,協助記住枯燥的臨床知識,方便於臨床實務中快速回想並應用,且不遺漏重要觀念細節。於多年臨床一對一衛教糖尿病患者過程中,得到許多的心得回饋,深感需要有一套周全性血糖控制策略,讓臨床工作者方便應用於第一線衛教指導,及糖尿病患能快速精準掌握自我照護的要點。自創發想出一個簡潔易懂的記憶口訣『FEED_ATOMS(進食_原子)原則』,提供周全性全方位高血糖控制策略,有助於臨床上醫護衛教指導病患及提供病患自我照護重點。
FEED ATOMS進食原子原則應用於血糖控制好比原子之於物質般,每個要素因子都是基礎且非常重要。落實飲食控制、運動、減重、規律使用藥物,每日每一餐每一口進食對於血糖控制是基本且重要的控糖原子原則。

方法
本文為敘述性回顧,以糖尿病血糖控制的臨床衛教重點及臨床實務,針對血糖衛教關鍵項目:糖尿病、血糖控制、飲食、運動、減重、藥物、食物總量、食物種類、進食順序、進食速度,以Pubmed資料庫搜尋相關文獻,闡述及歸納出臨床血糖控制的衛教原則。
〈相關影片:進食順序降餐後高血糖超商早餐如何吃?〉
討論
第二型糖尿病控制血糖最重要的四要素『FEED』:食物(food) 、運動(exercise)、減重(eliminate weight/fat)、與藥物(drugs)。其中飲食控制的四個因子「ATOMS」:餐食的總量、種類、順序及進食速度(amount, type, order of meals and eating speed),共同組成英文縮寫為:『FEED_ATOMS(進食_原子)原則』。
『FEED_ATOMS(進食_原子)原則』八大要素因子介紹
一、食物(Food)
糖尿病前期和糖尿病患者的飲食模式,強調關鍵的營養原則,包括:盡可能攝取非澱粉類蔬菜、適度攝取整顆水果(非果汁)、豆類、全穀物、堅果和乳製品,並減少攝取過量肉類、含糖飲料、精製穀物和超加工食品。
建議糖尿病患者和高風險族群盡可能用水、低熱量或無熱量飲料取代含糖飲料(包括果汁),以控製糖尿病並降低心臟代謝疾病的風險。
地中海飲食與低醣原則的結合
建議糖尿病患者考慮採用地中海飲食(Mediterranean diet) 1,2,這種飲食模式富含單元不飽和脂肪、多元不飽和脂肪及長鏈脂肪酸,取代飽和脂肪酸,如:蔬菜、水果、堅果、全穀物、魚類和橄欖油,以改善葡萄糖代謝、減少發炎反應,改善內皮細胞功能,並降低心血管疾病的風險。此外,建議搭配低醣飲食(low-carbohydrate diet, LCD)原則以控制血糖,即低醣地中海飲食(low-carbohydrate Mediterranean diet),更可有效控制血糖。地中海飲食不僅是一種飲食模式,更是一種生活方式,結合了運動和健康的飲食習慣。除了健康的飲食習慣外,規律的運動、避免吸菸、控制體重等因素,也都對減少血管發炎至關重要。
醣類攝取對血糖的影響
第二型糖尿病是醣類代謝異常的疾病。三大營養素包含醣類、蛋白質、脂肪,而使血糖增高的主要影響來自醣類,減少醣類攝取,可達降低血糖的目標。
美國糖尿病協會已將餐後血糖(postprandial glucose,PPG)確定為糖化血色素 (HbA1c)和糖尿病併發症的獨立影響因素,並且越來越多的證據表明,HbA1c、空腹血糖(fasting plasma glucose,FPG)和餐後血糖(PPG)這三個血糖參數均獨立且重要。減少飲食中碳水化合物的含量或增加可溶性纖維的攝取量(每1,000kcal至少含有14g纖維)可減少餐後血糖波動幅度。
〈延伸閱讀:如何降低餐後血糖?! 良好進食順序可達成!!〉
〈延伸閱讀:糖化血色素(HbA1c)是什麼?帶你掌握血糖控制的關鍵!〉
飲酒對血糖的影響與注意事項
有關飲酒,日本研究(Yamamoto等人, 2021)研究發現同時攝取葡萄糖和酒精,比單獨攝取葡萄糖,容易導致低血糖。因為同時攝取酒精和葡萄糖,會導致人體血糖濃度快速上升,增加胰島素分泌,最終導致血糖降低,甚至發生低血糖。可能是由於葡萄糖代謝產生的菸鹼醯胺腺嘌呤二核苷酸(nicotinamide adenine dinucleotide)促進了肝臟對酒精的代謝。個體對酒精的代謝能力、胰島素分泌能力和胰島素阻抗程度可能影響血糖代謝反應。酒精攝取量和方式也可能影響血糖代謝。建議適量飲酒,並避免空腹飲酒。建議對糖尿病患者進行飲酒後遲發性低血糖(delayed hypoglycemia)的症狀、徵兆和自我管理的教育,特別是在使用胰島素或胰島素促泌劑(insulin secretagogues)時。應強調飲用酒精性飲料後監測血糖的重要性,以減少發生低血糖的風險。
〈延伸閱讀:長期血糖穩定控制的關鍵因素有那些?減緩胰島細胞衰退很重要!〉
二、運動(Exercise)
身體活動不足是內臟脂肪堆積的一個獨立且強大的危險因素。建議糖尿病患者長時間久坐時應每30分鐘起身活動,以改善血糖。建議糖尿病患者,特別是青少年,每天應進行至少60分鐘的中等至高強度有氧運動,並包含每週至少3天的肌肉和骨骼強化活動。若活動量低於這個標準,則可被視為身體活動不足。堅持規律的有氧運動和力量訓練不僅有助於血糖控制,還可顯著提升情緒穩定、減輕壓力水平、改善認知功能以及減少炎症反應。同時,這些活動還能幫助維持神經傳導物質的穩定和平衡,有效提升整體健康狀況。
〈延伸閱讀:逆轉糖尿病!FEED ATOMS進食原子原則逆轉神經傳導失衡 〉
〈延伸閱讀:逆轉糖尿病:破解粒線體功能異常與活性氧物質的秘密 〉
缺乏運動與疾病風險的關聯
缺乏身體活動與第二型糖尿病患者較高的總體死亡率和心血管疾病風險有顯著關聯。與身體活動程度較高者相比,身體活動程度較低者的總體死亡率風險比(HR)為 1.41 (95% 信賴區間 [CI] 1.16–1.72)。規律運動可能和內臟脂肪量減少有關,可以預防許多與慢性發炎相關的疾病,例如:肥胖症及第二型糖尿病。
從不活動增加到每週 150 分鐘中等強度有氧運動,與較高的 CVD 風險呈負相關 (RR=0.83; 95% CI 0.77–0.89)。
〈延伸閱讀:運動時人體能量系統有哪些? 快速搞懂運動三大能量系統!〉
〈延伸閱讀:戴口罩運動對心率、血氧飽和度及呼氣末二氧化碳有什麼影響?Meta-analysis分析一次看!〉
建議的運動類型與時間
建議糖尿病的成年人每週進行150分鐘以上的中等強度或至少75 分鐘的高強度有氧運動,可增加肌肉對葡萄糖的攝取,如快走、慢跑、游泳和騎自行車等。每週阻力運動2-3次,增強骨骼肌質量,每個動作重複 8-12 次,做 2-3 組,例如舉重、阻力帶、徒手訓練:伏地挺身、深蹲等。每週進行2-3次彈性(flexibility)和平衡訓練(balance training),如瑜伽、太極拳,以增加靈活性、肌肉力量和平衡。運動前應諮詢醫生或物理治療師,根據自身情況調整運動強度和頻率。運動過程中應注意安全,避免受傷。
〈延伸閱讀:什麼運動降血糖效果最好?給糖尿病患者降血糖運動的建議〉
〈延伸閱讀:揭開超強體適能的密碼:睡眠心率 30 與儲備心率 150 的強悍真相〉
身體活動(Physical activity)和適度減重及生活方式改善,可將高風險族群的第二型糖尿病風險降低高達58%。 結合有氧運動和阻力運動比起單純只做有氧運動,可降低心血管疾病發病率和死亡率及微血管併發症,並改善HbA1c。各類運動的機制如下:
-
有氧運動:增加肌肉對葡萄糖的攝取,骨骼肌會促進GLUT-4(一種重要的葡萄糖轉運蛋白)轉位到細胞膜,以增加不依賴胰島素的葡萄糖攝取,可以降低空腹血糖和平均血糖濃度,並增加胰島素敏感性,效益可持續長達約 48 小時,有助於減少體脂,特別是內臟脂肪 ,這類運動包括快走、慢跑、游泳和騎自行車等。有氧運動在第二型糖尿病患可使糖化血色素HbA1c降低,平均差異 (MD): −0.71% [95% CI −1.11, −0.31]; p value = 0.0005,每增加一週運動時間,HbA1C%可額外降低約 0.009至0.04%( p = 0.002) 。胰島素阻抗(HOMA-IR)顯著改善,平均差異 (MD): −1.02[95% CI −1.77, −0.28]; p value = 0.007。空腹血糖顯著降低,平均差異 (MD): −12.53 mgl/dL[95% CI −18.94, −6.23]; p value <0.0001。空腹胰島素顯著改善,平均差異 (MD): −10.39 IU[95% CI −17.25, −3.53]; p value = 0.003。較長期間的持續運動HbA1c%的降低效果更佳顯著。
-
阻力訓練:增強骨骼肌質量。一項針對超過 8500 名第二型糖尿病患者進行的meta-analysis發現,阻力訓練使 HbA1c 顯著降低了 -0.57%,阻力運動阻可能不顯著影響空腹血糖,益處主要在降低餐後血糖。
-
結合訓練(有氧運動加阻力訓練):有氧運動、阻力訓練和結合訓練皆可改善血糖控制、肥胖及胰島素阻抗性。三種運動模式都能使HbA1c 降低。對於持續時間少於12 週的訓練,平均Hb A1c 降低了 0.8 ± 0.3%。其效果與飲食、藥物和胰島素治療的長期效果相似(0.6-0.8%)。結合訓練對空腹血糖、體重、高密度脂蛋白膽固醇和舒張壓有更大的益處。
〈延伸閱讀:正常人運動後血糖上升還是下降?運動完上升正常嗎?深入剖析!〉
〈延伸閱讀:運動健康不傷身!! 醫療級運動處方專為中高齡與慢性病患打造!〉
三、減重/減脂(Eliminate weight/fat)
肥胖的定義為脂肪在人體各部位或組織器官過度堆積。脂肪組織透過各種發炎機制及釋放更多游離脂肪酸導致胰島素阻抗。糖尿病是身體無法產生足量的胰島素或胰島素阻抗增加,組織無法有效利用胰島素,造成血糖上升。許多研究證實第二型糖尿病發生率與肥胖有重要關聯性。
BMI 與腰圍對疾病風險的影響
肥胖者身體質量指數 (body mass index, BMI)過高,過多的腹部脂肪、脂肪組織造成胰島素阻抗增加及影響β細胞的功能,罹患第二型糖尿病的風險隨著BMI的增加而線性增加。BMI 高於 20 kg/m² 與冠狀動脈心臟病(coronary heart disease, CHD) 存在強烈關聯性,且沒有觀察到性別的差異。腰圍可更精確的評估體脂肪分佈,內臟脂肪有較高的代謝心臟風險(cardiometabolic risk)。亞洲人較易產生腹部(內臟性)肥胖,對於胰島素抗性及第二型糖尿病,腰圍比BMI是更準確的預測指標。
〈延伸閱讀:減重的一般原則一次看!正餐營養要均衡,非正餐多餘熱量需先戒除!!〉
〈延伸閱讀:456健康瘦!漸進式低醣飲食(HBWRPLCD)減重控糖一次達標!!〉
亞洲族群的 BMI 標準
WHO 亞太地區將 BMI ≥ 23 kg/m² 定義為過重,BMI ≥ 25 kg/m² 定義為肥胖,這個標準主要考量到亞洲族群即使在較低的 BMI 值下,仍有較高的疾病風險。
減重對第二型糖尿病的益處
在過重或肥胖的第二型糖尿病患者,適度減輕5-10%的體重,可使HbA1c降低0.5%、收縮壓降低5mmHg、舒張壓降低5mmHg、HDL增加5mg/dl、三酸甘油脂降低40mg/dl,而減輕10-15%體重具有更大的益處。
2018年發表於The Lancet的DiRECT研究顯示,進行體重管理能有效緩解第二型糖尿病,研究的糖尿病緩解定義為『回到了非糖尿病狀態並停止使用降血糖藥物』。研究結果遠超過預期,在 12 個月時,干預組中近半數 (46%) 參與者達成了非糖尿病狀態並停用了抗糖尿病藥物。糖尿病緩解率與減重程度密切相關,減重5-10公斤者,有34%達成緩解,減重10公斤以上者,有73%達成緩解,減重15公斤以上者,緩解率更高達86%。
〈延伸閱讀:如何逆轉糖尿病?!〉
四、藥物(Drugs)
糖尿病的治療首重生活型態改變,包含:飲食控制、增加身體活動、減重/減脂,為最基本且重要的治療基礎。
藥物治療包含口服藥物:Metformin, Sulfonylureas, Glinides, α-Glucosi
dase inhibitors, Thiazolidinediones(TZD), Dipeptidyl peptidase 4 inhibitors(DPP-4Is), Sodium-Glucose Transport Protein 2 Inhibitors (SGLT-2Is)。
針劑:Insulin, Glucagon-Like Peptide-1 Receptor agonists(GLP-1Ras), Amylin agonists (pramlintide).
SGLT-2Is降低血糖、降低體重、降低血壓,顯著改善第二型糖尿病患者的心血管和腎臟預後。
GLP-1Ras降低血糖、降低體重、降低血壓。已證實能顯著降低major adverse cardiovascular events (MACE) 、心血管死亡、心肌梗塞和中風的風險,尤其在合併已有動脈粥狀硬化性心血管疾病的患者中有益處。GLP-1RAs 在具有心血管風險的第二型糖尿病患者的管理中佔有重要的地位。
註:major adverse cardiovascular events (MACE)包含coronary artery disease (CAD), cerebrovascular disease, and heart failure.
〈延伸閱讀:糖尿病藥物治療的目的是什麼?最齊全的降血糖藥物大解析!〉
低醣飲食與藥物調整的重要性
當第二型糖尿病患者改變飲食,特別是採用低醣飲食時,醫師應根據患者情況適當調整糖尿病藥物,以降低低血糖的風險。相對安全且可以持續使用的藥物包括Metformin、DPP-4Is,以及GLP-1Ras。SGLT-2Is這類排糖藥物應停止使用,以避免發生血糖正常的酮酸中毒(euglycemic diabetic ketoacidosis)。此外,像Sulfonylureas、Glinides及α-Glucosidase抑制劑等藥物也需考慮減量或停用。基礎長效胰島素(basal long-acting insulins)則須適當減少劑量,而複方胰島素(例如70/30配方)可以考慮改為基礎長效胰島素。當使用固定胰島素劑量時,應向個人提供有關碳水化合物攝取時間和份數(serving)的教育,同時考慮胰島素作用時間,可以改善血糖並減少低血糖風險。已使用降血糖藥物者開始進行低醣飲食,宜1-2週就進行追蹤一次血糖,並視情況調整藥物劑量。
〈延伸閱讀:連續血糖監測(CGM)怎麼用?掌握原理,血糖控制不再難!〉

五、總量(Amount) 及 種類(Type)
依照衛生福利部國民健康署之『每日飲食指南手冊』,六大類食物中含醣比例較高、容易造成餐後血糖偏高的為:全穀雜糧類、水果類。食用這二類食物時應注意攝取總量,以減少血糖上升的幅度,亦即選擇高升糖指數(Glycemic Index, GI)食物,控制好攝取總量,即可控制升糖負荷(Glycemic Load, GL)值不過高,進而減少血糖上升幅度。
血糖和醣類的攝取量有關,攝取過多的醣類,除了升高血糖,也會轉成脂肪堆積在肝臟及胰臟,造成胰島素阻抗。因此,減少醣類攝取,減少胰島素分泌,除改善血糖,也促進脂肪酶將脂肪組織中的三酸甘油酯釋放出脂肪酸作為能量來源(lipolysis and fatty acid oxidation),減少肝臟及胰臟脂肪堆積,移動及代謝脂肪,並減少脂肪新生(de novo lipogenesis),使體重減輕;並因減少糖毒性、減少氧化壓力及發炎,使胰臟功能正常化,有機會逆轉第二型糖尿病。
低醣飲食的標準
一般以每日攝取醣類≦130克(或總能量的25%以下)為低醣飲食、≦50克(或總能量<10%)為極低醣飲食(Very low carbohydrate diet, VLCD) 。
醣類飲食分類比較表
| 飲食名稱(Diet name) | 醣類量(Carbohydrate amount) |
|---|---|
| 高醣(High carbohydrate) | ≧45%總熱量,≥225 克/天 |
| 中醣(Moderate carbohydrate) | 26-44% 總熱量,131-224 克/天 |
| 低醣(Low carbohydrate) | 10-25% 總熱量,51-130 克/天 |
| 極低醣(Very low carbohydrate) | < 10%總熱量,≦ 50克/天 |
| 極低醣生酮飲食(Very low carbohydrate ketogenic) | 如上,但蛋白質通常限制≦20%總熱量,血中酮酸介於0.5-5 mmol/L |
| (1) 計算是基於每日2000大卡總熱量 (2) 酮酸(BOHB): β-hydroxybutyrate |
|
在本土為期18個月的研究中,以每日90克的低醣飲食,較符合國人飲食的習慣,低醣組比傳統糖尿病飲食組有較佳的血糖控制、減少糖尿病用藥、降低體重、減少腰圍、臀圍及下降血壓;不影響膽固醇、小緻密性低密度脂蛋白膽固醇(sdLDL-C)、尿蛋白、腎功能、肝功能及頸動脈動脈硬化(carotid atherosclerosis)。
日本的研究發現每日130克低醣飲食平均糖化血色素下降約0.8%,每日90克低醣飲食平均糖化血色素下降約1.6%,小於50克的極低醣飲食可下降2.6%。
〈延伸閱讀:456健康瘦!漸進式低醣飲食(HBWRPLCD)減重控糖一次達標!!〉
GI值和GL值差別
-
升糖指數(Glycemic Index, GI),簡稱GI值:食用100公克葡萄糖後2小時內的血糖增加值為基準(GI值=100),來比較各類食物攝取2小時內血糖上升的面積,當上升面積越大,代表GI越高,用來衡量各種含醣食物影響血糖程度的指數。低(GI≦55)、中(55 < GI < 70)、高(GI≧70),GI值越高對血糖影響越大。攝取GI值越高的食物,造成血糖上升速度及幅度越大、胰島素分泌過多,脂肪合成增加,不利於血糖控制及減重16。
-
升糖負荷(Glycemic Load, GL),簡稱GL值:計算方式為「食材的碳水化合物含量(公克) × GI值 ÷ 100」,考慮的不只是食物的GI值,而是攝取的碳水化合物總量,更能精準地瞭解一份飲食使血糖上升的程度。澳洲雪梨大學線上資料庫對於GL範圍的定義:低(GL≦10)、中(10 < GL < 20)、高(GL≧20),GL值越高對血糖影響越大。
研究發現攝取高 GI 值和高 GL值 的食物與第二型糖尿病和心血管疾病的風險增加有關聯。攝取高 GI 值食物與第二型糖尿病的發生率增加有關聯(RR 1.27 [95% CI 1.21–1.34]; p<0.0001),高 GI 值食物也與總體心血管疾病(包括死亡率)的發生率增加有關聯 (RR 1.15 [95% CI 1.11–1.19]; p<0.0001),高 GL值 與第二型糖尿病有相似的關聯 (RR 1.15 [95% CI 1.09–1.21]; p<0.0001),高 GL 值也與總體心血管疾病有相似的關聯 (RR 1.15 [95% CI1.10–1.20]; p<0.0001)。在飲食建議中降低 GI值 和 GL值 的做法,其對健康結果(包括第二型糖尿病和心血管疾病)的影響,可能與建議增加纖維和全穀物攝取的效果相似。
〈延伸閱讀:升糖指數及升糖負荷是什麼?搞懂 GI、GL值,控糖、瘦身一次搞定〉
六、順序(Order of meals)
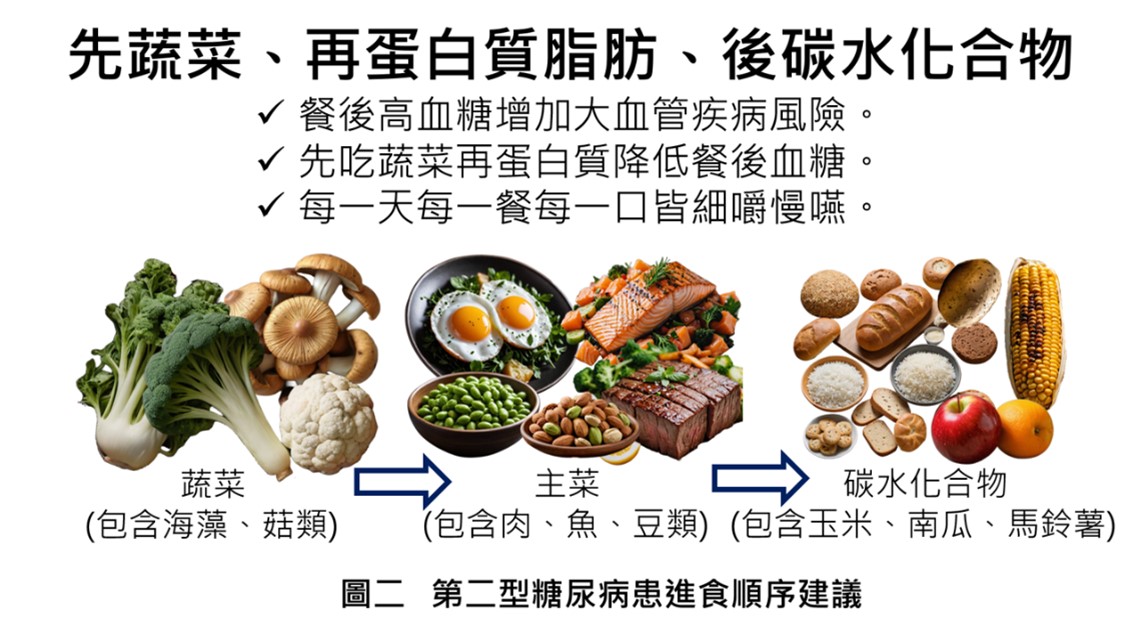
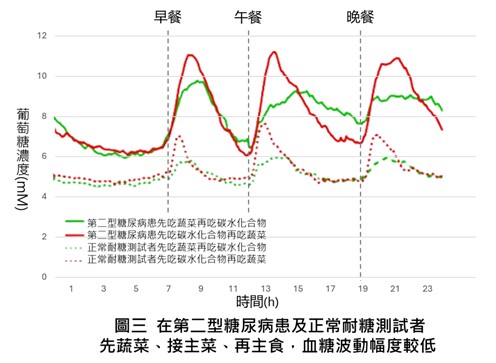
餐後高血糖(postprandial hyperglycemia)會增加心血管疾病風險,依照醣類最後吃(carbolast)的概念:先吃蔬菜類等高膳食纖維食物(含海藻和菇類等),接著豆魚蛋肉類蛋白質主食,再吃醣類食物(含五榖雜糧類,包括:米飯、麵食、麥片、麵包、馬鈴薯、山藥、南瓜、芋頭、地瓜、玉米、水果等),有助於降低餐後高血糖,對於短期血糖波動和長期血糖控制皆有效。
對於非糖尿病患者的正常人,其血糖波動、餐後血糖和胰島素水平亦顯著降低 。
在蔬菜和肉類之後,最後攝取醣類,可以防止餐後血糖和胰島素的波動。
〈延伸閱讀:如何降低餐後血糖?! 良好進食順序可達成!!〉
七、速度(Speed)
自訴快速進食與罹患第二型糖尿病的風險可能有關。
胃需要大約 20 分鐘來向大腦發出飽足信號,快速進食可能導致大腦來不及接收到飽足感信號,造成過度飲食。快速進食減少咀嚼時間,導致更高的血糖濃度及血糖快速波動,可能導致胰島素阻抗。快速進食可能誘發特定的細胞激素,如白細胞介素-1β(interleukin-1β)和白細胞介素-6(interleukin-6),會增加胰島素阻抗。健康女性的快速飲食與較高的血糖波動有關。
進食速度是一個可改變的風險因子,因此緩慢進食可能可以減少糖尿病風險。進食速度影響腸道飽足感激素,緩慢進食會增加 peptide tyrosine-tyrosine (PYY)並減少ghrelin分泌,增加飽足感並減少食物攝取,可能有助於第二型糖尿病人短期飯後血糖及胰島素控制。
FEED控糖五要素及ATOMS飲食控制四原子總結
【Food食物】控制餐後血糖為控糖重要指標。關鍵在飲食控制四原子「ATOMS」。
【Exercise運動】:規律運動(有氧及重量訓練)可改善胰島素阻抗、降低HbA1c、空腹及餐後血糖。
【Eliminate weight/fat減重/減脂】:減重5-10%降低HbA1c、降血壓。減重是逆轉糖尿病關鍵!!
【Drugs藥物】:降血糖藥物,於低醣飲食應考慮調整劑量以避免低血糖。積極用藥可延緩胰島β細胞衰退。
【Devices裝置】:CGM及時飲食、運動、 藥物個人化反饋,助血糖達標。GPS運動錶輔助運動體適能管理。
【Amount總量】:減少醣類總量攝取,達成低 GL 值飲食以改善血糖。
【Type種類】:醣類(含水果、高醣飲料),容易餐後高血糖,優先挑選低GI醣類食物。
【Order of Meals順序】:蔬菜類→豆魚蛋肉類→醣類,降低整體GI值並增加飽足感,降低餐後血糖及胰島素。
【Speed速度】:減緩進食速度有助降低餐後血糖及胰島素分泌。
〈看更多:衛教單下載〉
結論
『FEED_ATOMS(進食-原子)原則』針對糖尿病血糖控制衛教提供周全性策略。包括:控糖關鍵四要素(FEED)及飲食控制四原子(ATOMS),血糖控制易達標,減少血管發炎及內皮功能障礙,預防及延緩動脈粥狀硬化,降低心血管疾病風險。在職場健康促進領域深受業界肯定及官方認可,糖尿病控糖要訣『FEED_ATOMS(進食-原子)原則』有學術界醫學實證,如果有任何職場健康方面需求,歡迎與我聯繫。看完本篇精華版,對於FEED ATOMS萌生興趣的讀者,歡迎點擊連結查看全篇論文。
參考文獻
-
綜論論文:糖尿病控糖要訣『FEED_ATOMS(進食_原子)原則』:控制高血糖及降低心血管風險
(Diabetes Glycemic Control Tips“FEED_ATOMS principle” :High Blood Glucose Control and Cardiovascular Risk Reduction)-
作者:陳承勤、林廷燦、陳晶瑩。
-
刊物:《內科學誌》2025:36:255-263。
-
核心內容:提出整合控糖五要素(FEED)與飲控四原子(ATOMS)的記憶口訣,強調落實於「每一天每一餐每一口」的周全性血糖管理策略。
-
-
綜論論文:第二型糖尿病的低醣飲食:從實驗室到臨床 (Low Carbohydrate Diet in Type 2 Diabetes Patients: from Bench to Bedside)
-
作者:陳晶瑩、何明華、陳慧君。
-
刊物:《內科學誌》2024;35:339-47。
-
核心內容:闡述低醣飲食的中心思想(低醣、中蛋白質、高脂肪、醣類最後吃)與病生理機轉,並提供實務性的醣類份數計算與安全性用藥調整原則。
-
-
臨床研究論文:Effect of a 90 g/day low-carbohydrate diet on glycaemic control... in type 2 diabetic patients: An 18-month randomised controlled trial
-
作者:Chin-Ying Chen(陳晶瑩), Wei-Sheng Huang(黃威勝), etc。
-
刊物:PLOS ONE 15(10): e0240158 (2020)。
-
核心內容:在台大醫院進行為期 18 個月的隨機對照試驗,證實每日 90 克(6 份醣)的中度低醣飲食(LCD)在血糖控制、藥物減量與減重成效上均優於傳統糖尿病飲食。
-
-
長期追蹤論文:The potential prolonged effect at one-year follow-up after 18-month randomized controlled trial... in patients with type 2 diabetes
-
作者:Chin-Ying Chen(陳晶瑩), Wei-Sheng Huang(黃威勝), Ming-Hua Ho(何明華), etc。
-
刊物:Nutrition and Diabetes (2022) 12:17。
-
核心內容:針對上述 18 個月試驗後的患者進行 12 個月(總計 30 個月)的追蹤,發現低醣飲食具有「潛在延續效應」,即使在試驗結束一年後,患者仍能維持較佳的血糖、藥物與肝功能指標。
-
欲大宗購買(10本以上)<逆轉糖尿病!>,視書籍訂購數量享有作者優惠折扣,若欲訂購書籍歡迎聯絡我們,書籍作者將依照書籍內面您希望書寫的字句,親筆簽名並寄送至指定地址。
〈相關影片:逆轉糖尿病!〉




